En bref
Détecter le cancer tôt, avant qu'il n'ait évolué vers une maladie métastatique et réfractaire au traitement, est essentiel pour améliorer les résultats des patients. Mais pour tirer parti de la détection précoce, il est nécessaire de prédire quels cancers à un stade précoce deviendront agressifs et de développer des stratégies thérapeutiques pour intervenir dans ce processus. Cela nécessite une nouvelle génération de biomarqueurs - molécules, changements génétiques ou autres indicateurs mesurables - qui peuvent indiquer la probabilité que les cancers à un stade précoce évoluent et s'ils répondront aux traitements. Cela exige également une compréhension approfondie des changements moléculaires et cellulaires qui conduisent à la tumorigenèse et provoquent la progression, posant les bases d'une nouvelle génération de thérapies curatives.
En utilisant notre technologie de pointe et en collaborant avec nos partenaires cliniques, nous avons développé un programme de premier plan pour découvrir comment les cellules cancéreuses précoces et leurs microenvironnements évoluent pour devenir agressifs, prédire quels cancers à un stade précoce sont à haut risque, et développer des biomarqueurs et des stratégies de médecine de précision pour correspondre aux patients avec des thérapies potentiellement curatives, y compris l'immunothérapie. Cette stratégie nous permettra de tirer parti des améliorations dans la détection précoce du cancer en optimisant le traitement pour intercepter les cancers à haut risque avant leur progression.
Domaines d'intérêt
Médecine de précision pour les cancers à un stade précoce. L'ICG ouvre la voie à la découverte de biomarqueurs dans les cancers à un stade précoce. Nos rôles de premier plan dans les réseaux de médecine de précision, avec des partenaires cliniques à travers le Canada, nous donnent accès à des collections uniques d'échantillons de patients et de données, notamment issues de grands essais cliniques de nouvelles thérapies contre le cancer telles que l'immunothérapie. Nous utilisons une technologie d'imagerie avancée, de l'intelligence artificielle et de l'apprentissage automatique pour découvrir de nouveaux biomarqueurs innovants basés sur l'abondance, les propriétés et les relations spatiales entre les cellules individuelles. Ces biomarqueurs peuvent prédire l'évolution du cancer, les réponses aux traitements et les résultats cliniques avec une précision sans précédent. Parallèlement, en utilisant une analyse pilotée par l'IA d'images de pathologie standard, nous révélons des caractéristiques cachées dans la structure du tissu tumoral qui peuvent améliorer la détection des cancers à un stade précoce, tels que le cancer du sein, et fournir une source riche de nouveaux et puissants biomarqueurs. En fin de compte, cette approche nous permet de capitaliser sur la promesse de la détection précoce du cancer en fournissant aux cliniciens les outils pour évaluer précisément le risque et associer chaque patient à la meilleure thérapie possible. Parallèlement, nos études précliniques de pointe sur les maladies à un stade précoce fournissent des connaissances fondamentales qui expliquent et renforcent les observations et découvertes du monde clinique, élargissant la gamme de nouvelles cibles et établissant un nouvel arsenal de thérapies pour éradiquer les cancers agressifs à un stade précoce.
Membres de l'équipe
Nos découvertes
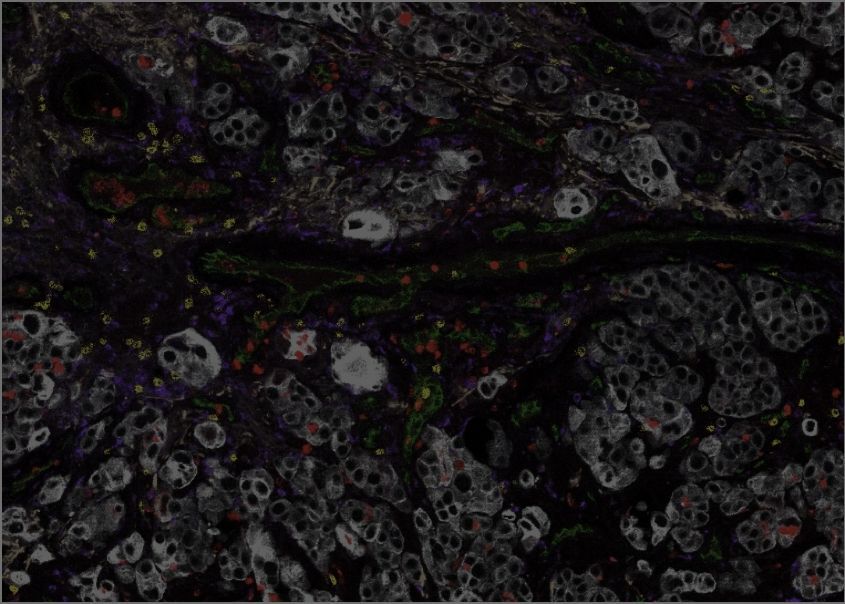
Nous avons mis au point une plateforme d'apprentissage automatique intégrant une forme avancée d'analyse d'image basée sur l'IA, connue sous le nom de vision par ordinateur, pour étudier de vastes ensembles de données générés à l'aide de notre technologie "omique" spatiale à cellule unique. En collaboration avec des partenaires au Centre universitaire de santé McGill (CUSM), le Réseau des centres d'oncologie du marathon de l'espoir de l'ITFR (Terry Fox Research Institute), le Consortium du cancer du Québec et le Réseau de recherche sur le cancer du poumon de McGill, nous avons utilisé cette technologie pour fournir une multitude de nouvelles informations sur l'organisation du microenvironnement immunitaire au sein des cancers du poumon. Cela a conduit à de nouveaux biomarqueurs prédisant lesquels des cancers du poumon réapparaîtront après une chirurgie, et quels patients atteints d'un cancer du poumon récurrent répondront le mieux à l'immunothérapie. L'ICG est un partenaire scientifique majeur de l'un des essais les plus importants au monde sur l'immunothérapie dans le cancer du poumon précoce, dans le cadre préchirurgical (« néoadjuvant »). Ce partenariat permet à notre technologie unique et à nos plateformes d'analyse de cibler les caractéristiques du microenvironnement immunitaire tumoral qui prédisent la réponse des cancers du poumon au stade précoce à ce traitement.
Forde P.M., Spicer, J., CheckMate 816 Investigators. Neoadjuvant Nivolumab plus Chemotherapy in Resectable Lung Cancer. New England Journal of Medicine. 2022 May 26;386(21):1973-1985.
Karimi, E., et al. Machine learning meets classical computer vision for accurate cell identification. bioRxiv 2022.02.27.482183
Sorin, M., et al., Single-cell spatial landscapes of the lung tumour immune microenvironment. Nature vol. 614, pp. 548–554 (2023).
Sorin, M. et al., Single-cell spatial landscape of immunotherapy response reveals mechanisms of CXCL13 enhanced antitumor immunity. J Immunother Cancer. 2023 Feb;11(2):e005545. doi: 10.1136/jitc-2022-005545. PMID: 36725085
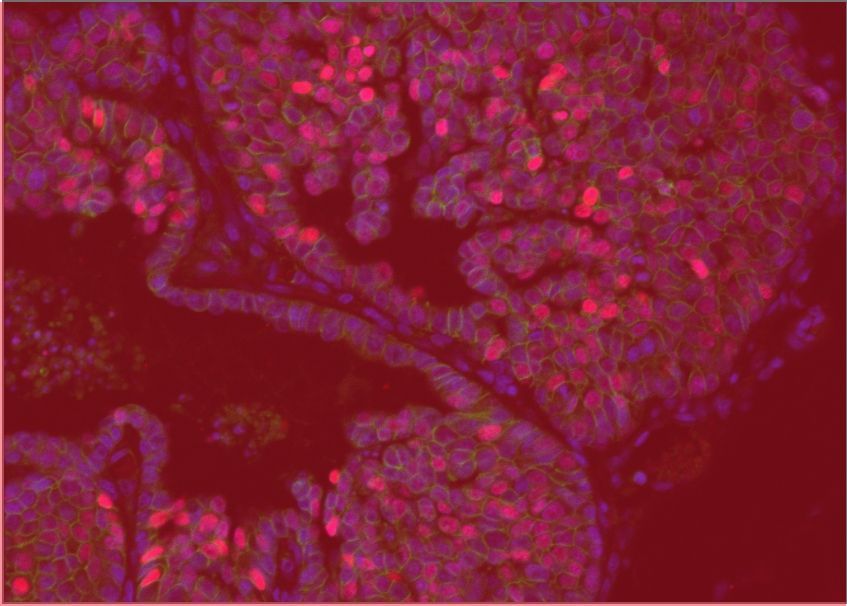
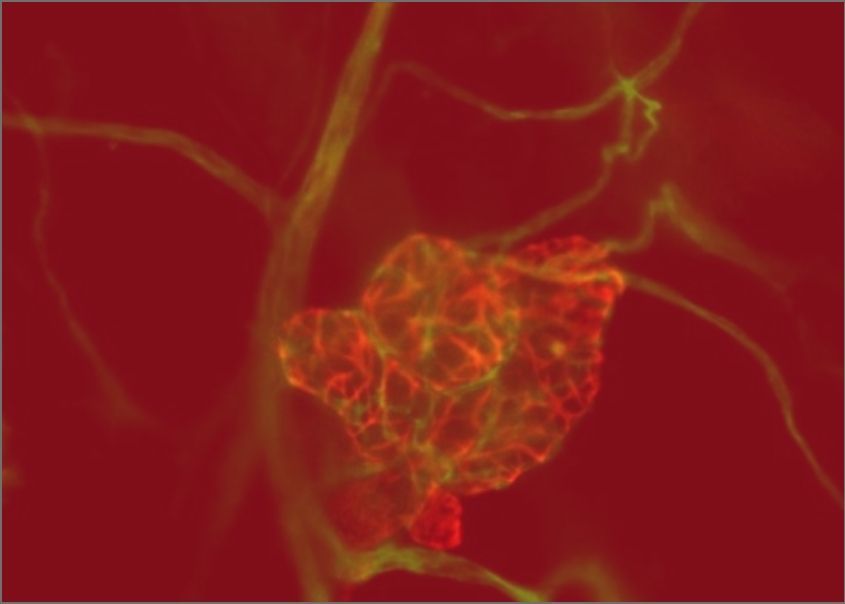
Une compréhension plus approfondie des premiers stades de la formation des tumeurs est nécessaire pour détecter et traiter les cancers alors qu'ils sont encore gérables. Les scientifiques de l'ICG ont utilisé des modèles innovants et des analyses à cellule unique pour révéler la cellule d'origine et les programmes génétiques clés du type le plus courant de cancer de l'ovaire. Leur travail a élargi nos connaissances fondamentales sur le développement du tractus reproducteur, tout en ouvrant la voie à de nouveaux traitements pour le cancer de l'ovaire, une maladie hautement agressive avec des options thérapeutiques limitées.
Teng, K., et al. Modeling High-Grade Serous Ovarian Carcinoma Using a Combination of In Vivo Fallopian Tube Electroporation and CRISPR-Cas9-Mediated Genome Editing. Cancer Research. 2021 Oct 15;81(20):5147-5160.
Ford, M.J., et al. Oviduct epithelial cells constitute two developmentally distinct lineages that are spatially separated along the distal-proximal axis. Cell Reports. 2021 Sep 7;36(10):109677.
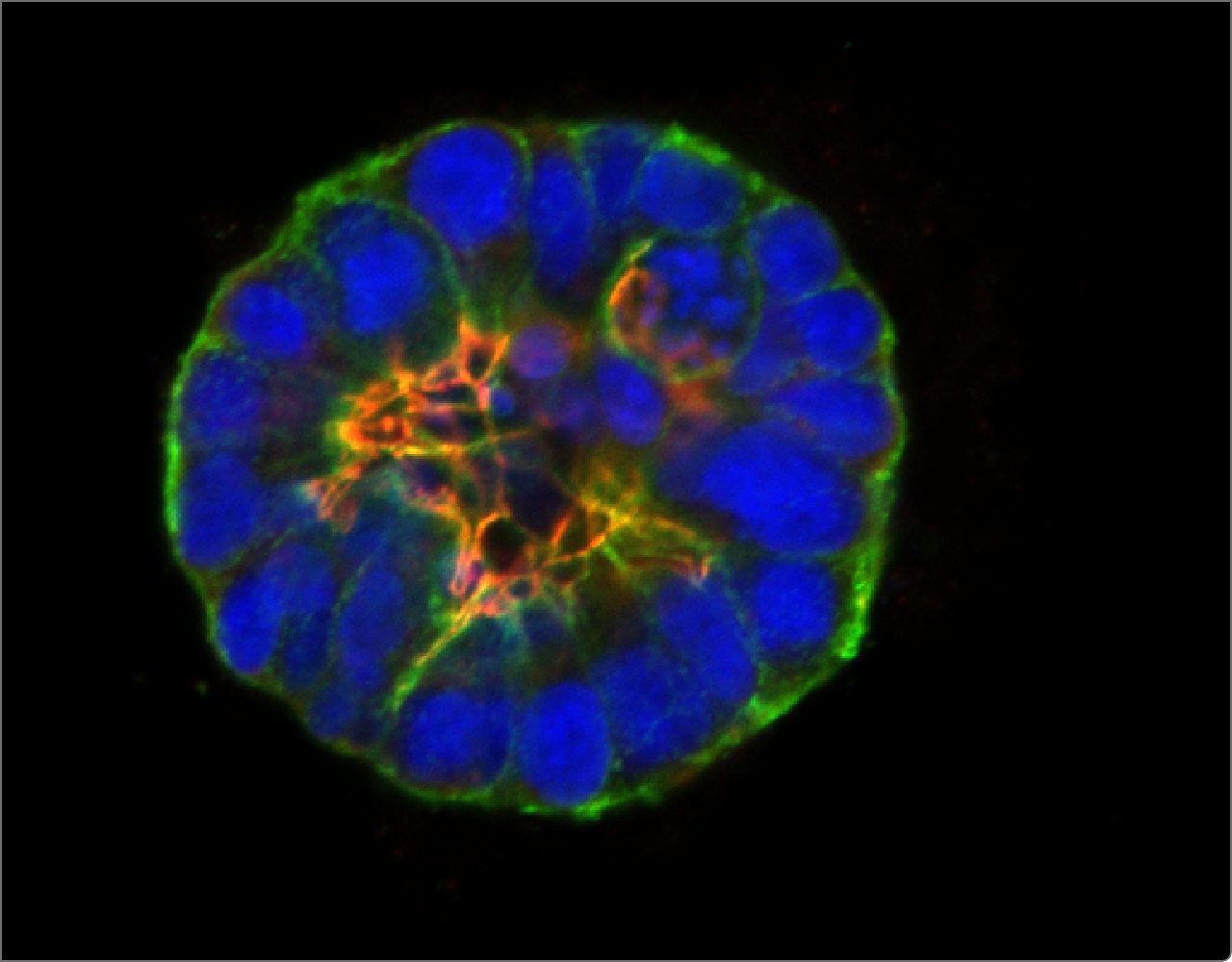
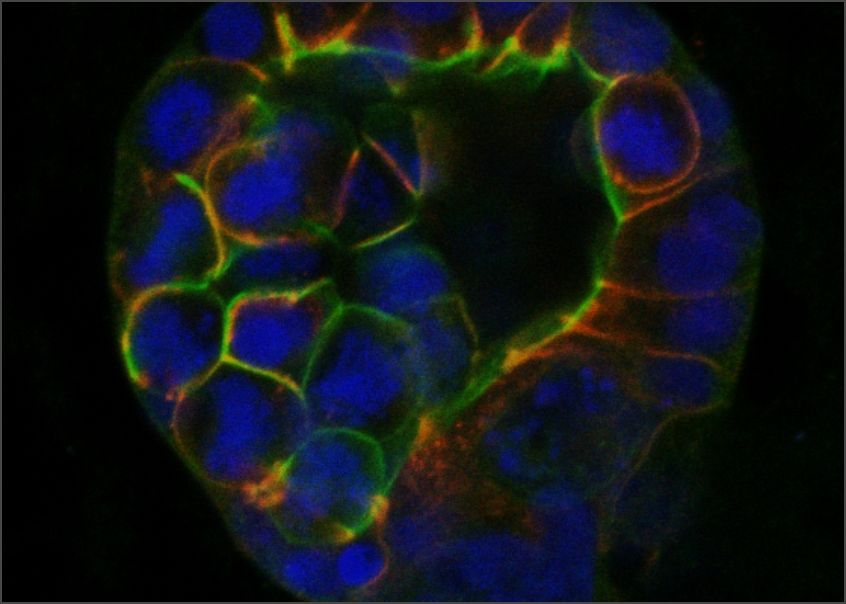
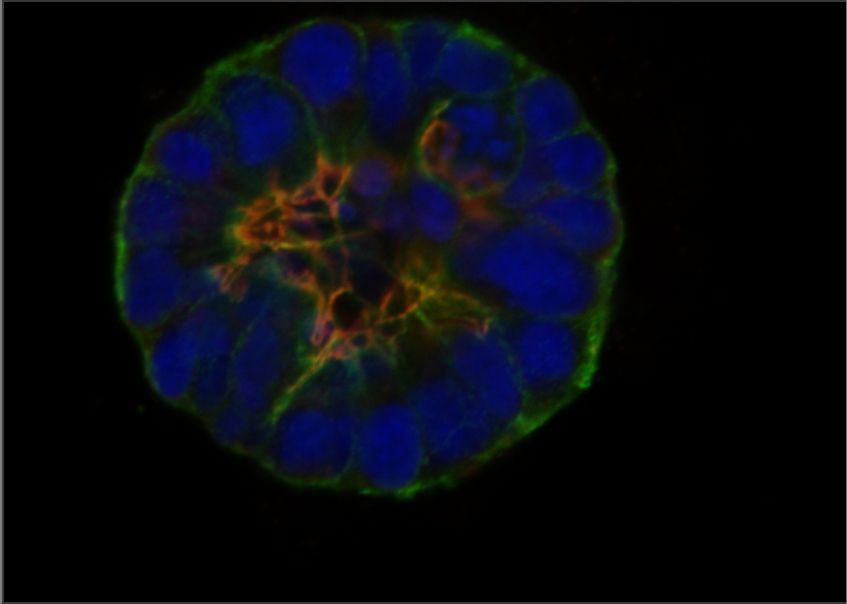
Les cellules organisent leur structure interne et leurs interactions mutuelles lors du développement normal des tissus, mais cette organisation (appelée polarité épithéliale) est perdue dans de nombreux cancers. Les chercheur.es de l'ICG ont joué un rôle essentiel en établissant que les premières étapes du développement du cancer du sein impliquent la perte de la polarité épithéliale et en révélant les mécanismes moléculaires impliqués.
McCaffrey, L.M., et al. Loss of the Par3 Polarity Protein Promotes Breast Tumorigenesis and Metastasis. Cancer Cell. 2016 Aug 8;30(2):351-352.
Halaoui, R. , et al. Progressive polarity loss and luminal collapse disrupt tissue organization in carcinoma. Genes & Development. 2017 Aug 1;31(15):1573-1587.
Wang, L.-T., et al. Rajah A, Brown CM, McCaffrey L. CD13 orients the apical-basal polarity axis necessary for lumen formation. Nat Commun. 2021 Aug 4;12(1):4697.
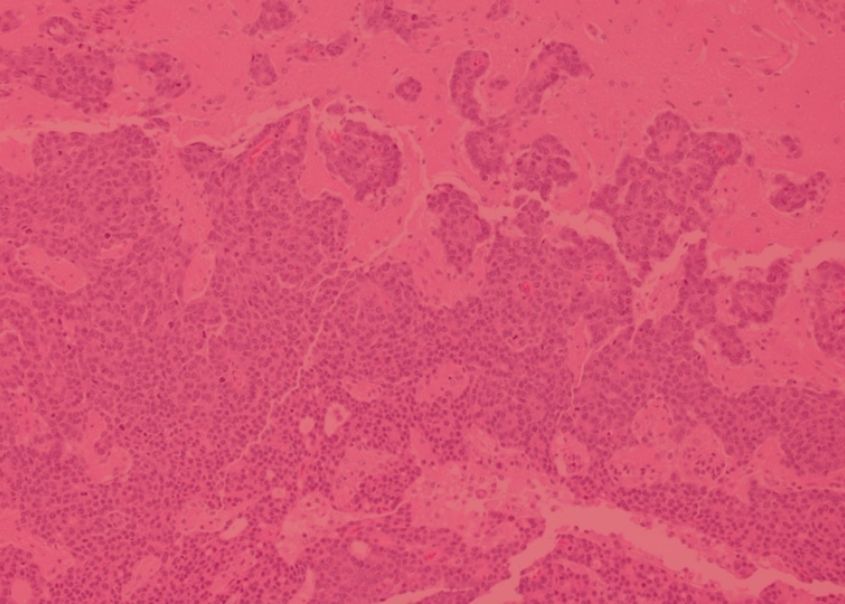
Le diagnostic du cancer repose largement sur l'analyse de l'anatomie microscopique des biopsies de tumeurs, un processus appelé histologie. Cette analyse est généralement réalisée manuellement par des pathologistes, mais les techniques assistées par ordinateur évoluent et sont sur le point d'accroître la rapidité et la précision du diagnostic du cancer. Les scientifiques de l'ICG collaborent avec des experts en intelligence artificielle pour développer des méthodes d'analyse d'images histologiques courantes à l'aide d'une technique appelée apprentissage profond. Leur travail améliore l'efficacité de la détection automatisée assistée par l'IA des cancers précoces et a montré des résultats prometteurs dans des échantillons de cancer du sein et du côlon, deux types de tumeurs pour lesquels l'analyse histologique des biopsies demeure la norme de référence pour le diagnostic.
Belharbi, S. et al. Deep Interpretable Classification and Weakly-Supervised Segmentation of Histology Images via Max-Min Uncertainty. IEEE Trans Med Imaging 2022 Mar;41(3):702-714. doi: 10.1109/TMI.2021.3123461