En bref
Les cancers présentant un taux de mortalité élevé comprennent généralement ceux diagnostiqués à un stade avancé, tels que le cancer du pancréas. D'autres cancers, comme le cancer du sein, constituent en réalité un spectre de sous-types uniques induits par des événements distincts et caractérisés par une biologie propre. Certains de ces sous-types sont plus facilement traitables, tandis que d'autres sont hautement agressifs et résistants aux traitements standard tels que la chimiothérapie. Les thérapies ciblées qui bloquent spécifiquement l'activité des protéines favorisant la croissance et la survie des sous-types de cancer agressifs peuvent être plus efficaces et plus sûres que les traitements précédents. Cependant, tous les mécanismes de cancer ne peuvent pas être ciblés par les stratégies conventionnelles de développement de médicaments. Certains cancers à mauvais pronostic sont également rares et peu étudiés, ce qui signifie que nous manquons de connaissances sur la manière de cibler ces tumeurs. Par conséquent, de larges groupes de patients ne bénéficient actuellement pas de thérapies ciblées. De plus, même les thérapies ciblées les plus avancées ne fonctionnent pas de manière égale pour tous les patients, les tumeurs ne répondant souvent pas comme prévu, ou répondant initialement mais rechutant ensuite ou réapparaissant sous forme de maladie résistante. La résistance au traitement est l'un des facteurs les plus importants limitant actuellement la survie et réduisant la qualité de vie des patients atteints de cancer. Elle est souvent associée aux métastases, le processus par lequel les cellules cancéreuses quittent leur site d'origine et se propagent à d'autres organes. Notoirement difficile à traiter, la maladie métastatique provoque plus de 90 % des décès liés au cancer et constitue une raison majeure du taux de mortalité élevé des cancers qui sont généralement diagnostiqués tardivement, lorsque la maladie métastatique est déjà établie.
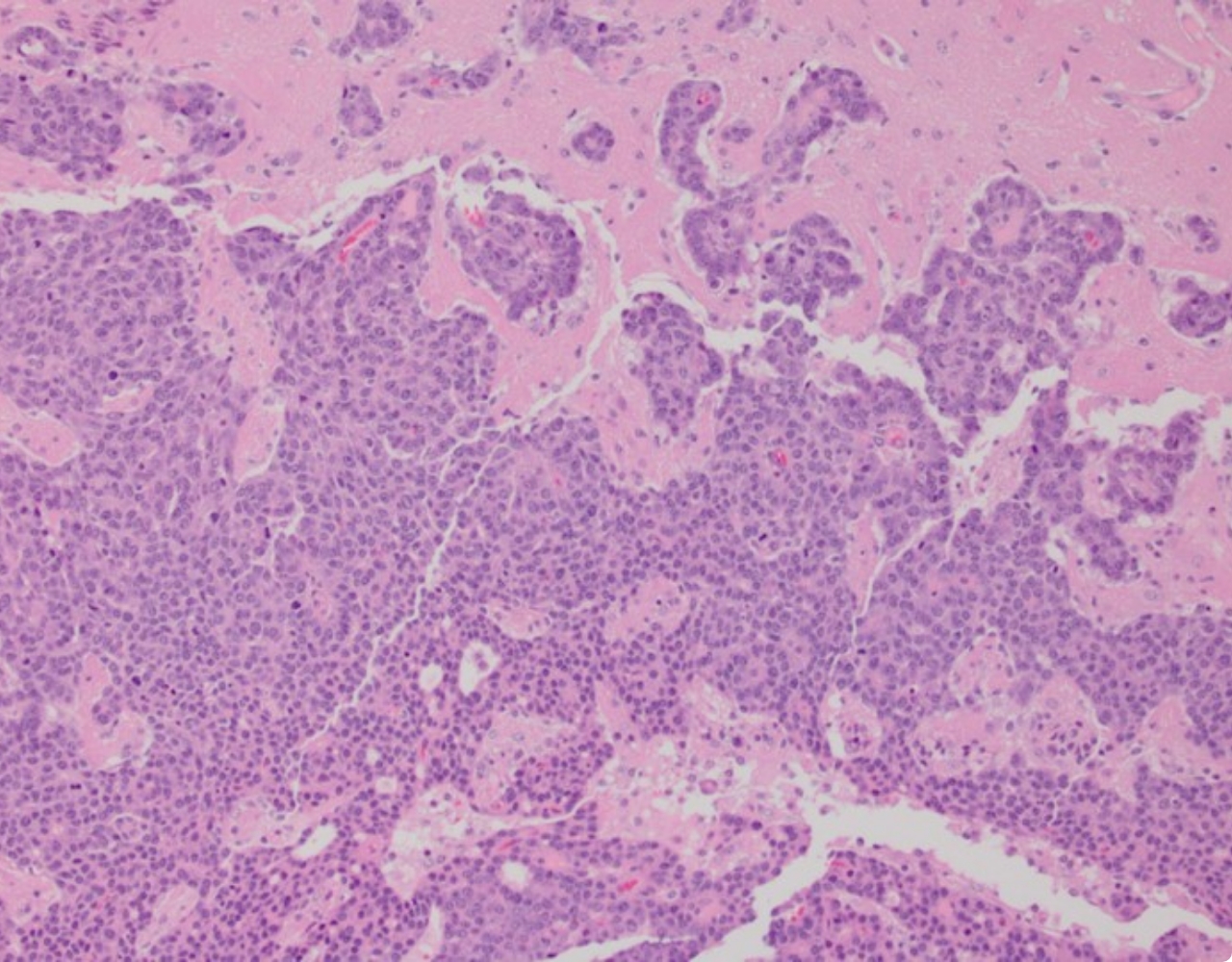
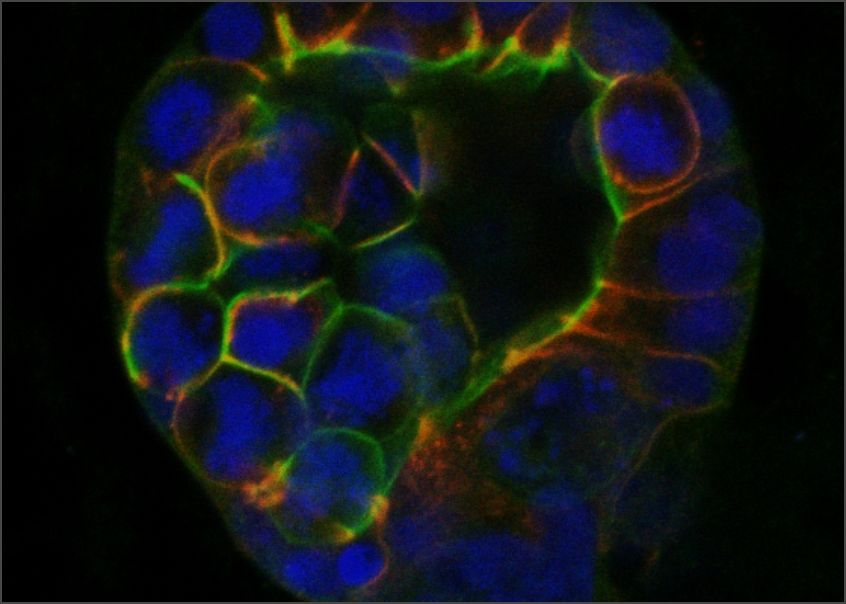
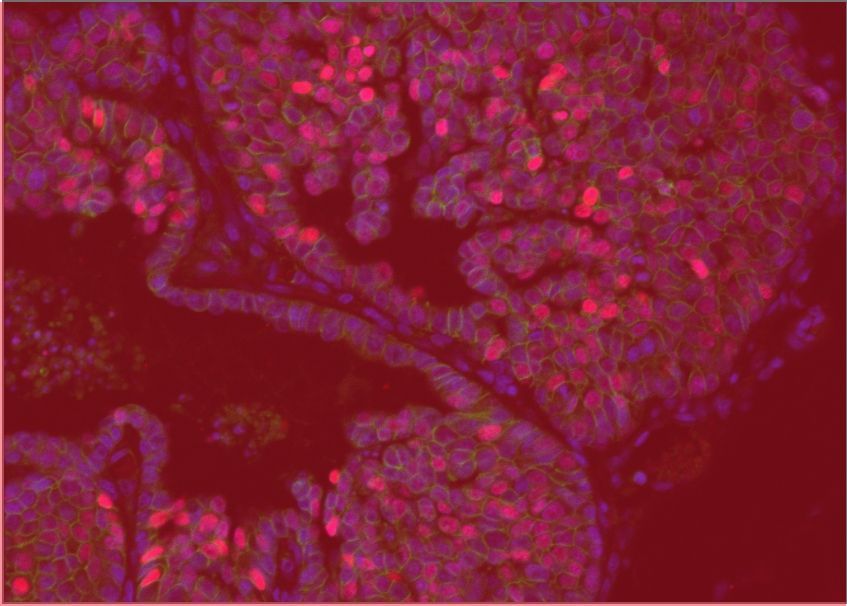
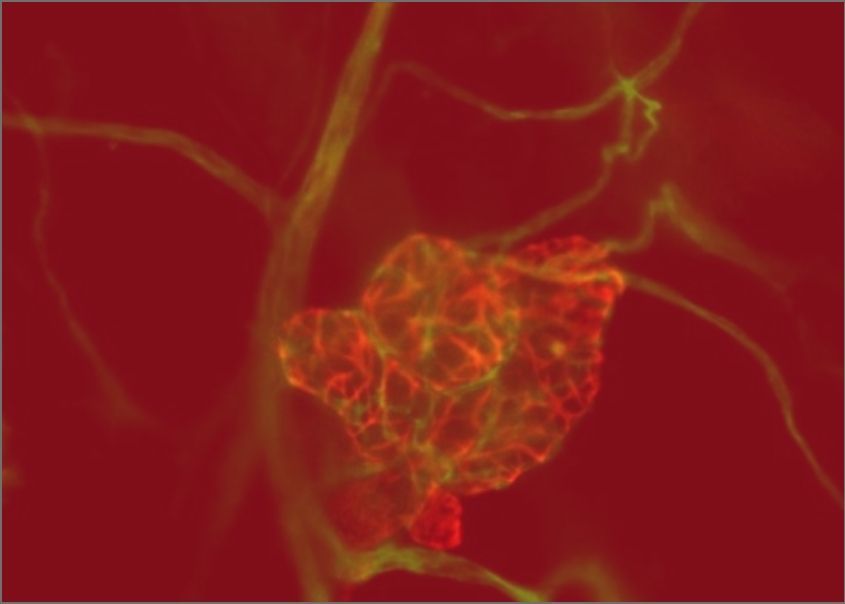
L'ICG est un point focal de réseaux et de consortiums dédiés à la médecine de précision. En appliquant des technologies de pointe et des méthodes analytiques à des collections uniques d'échantillons cliniques et de données, nous révélons les caractéristiques génomiques, moléculaires et cellulaires associées à la progression métastatique et à la résistance aux thérapies. Nous avons mis au point des techniques avancées pour recréer les caractéristiques des cancers à taux de mortalité élevé chez des organismes modèles avec un microenvironnement totalement intact, ainsi que des technologies pour faire croître des tumeurs en laboratoire directement à partir d'échantillons prélevés chirurgicalement sur des patients. Ces modèles de cancer hautement précis nous permettent de découvrir les mécanismes et les vulnérabilités sous-jacents aux maladies résistantes et métastatiques et de les comprendre à un niveau fondamental, ouvrant la voie à des stratégies thérapeutiques nouvelles et plus efficaces pour les cancers à taux de mortalité élevé.
Domaines d'intérêt
Membres de l'équipe
Our Discoveries
L'hypothèse du "semis et du sol" est une idée ancienne expliquant les schémas de métastases observés cliniquement, selon lesquels certains types de cancers métastasent de manière préférentielle vers des organes secondaires spécifiques. Cette hypothèse avance que cela ne se produit pas par hasard, mais parce que chaque type de cellule cancéreuse est adapté pour survivre et se développer uniquement dans des microenvironnements spécifiques. Les travaux réalisés à l'ICG ont offert un aperçu sans précédent de ce phénomène en déterminant comment les cellules cancéreuses régulent de manière unique leurs programmes génétiques et métaboliques lors de la métastase vers différents organes. Cela a éclairé de nouveaux aspects sur les mécanismes de métastases spécifiques au site, identifiant des vulnérabilités ciblables dans le processus métastatique à chaque site. En s'appuyant sur des observations issues d'études cliniques et précliniques, nos chercheur.es ont également développé des modèles génétiquement modifiés qui ont mis en évidence l'implication de gènes spécifiques dans la métastase dans le contexte d'un microenvironnement entièrement intact, comprenant le système immunitaire et tous les autres types de cellules stromales. Les résultats de ces études ont conduit au développement de stratégies thérapeutiques, dont certaines ont été testées dans des essais cliniques, avec le potentiel de transformer les résultats pour les cancers à forte mortalité en bloquant la métastase.
Osteoactivin promotes breast cancer metastasis to bone. Rose AA, et al. Mol Cancer Res. 2007 Oct;5(10):1001-14. doi: 10.1158/1541-7786.MCR-07-0119. PMID: 17951401
Phase I/II study of the antibody-drug conjugate glembatumumab vedotin in patients with locally advanced or metastatic breast cancer. Bendell J, et al., J Clin Oncol. 2014 Nov 10;32(32):3619-25. doi: 10.1200/JCO.2013.52.5683. Epub 2014 Sep 29. PMID: 25267761
Claudin-2 is selectively enriched in and promotes the formation of breast cancer liver metastases through engagement of integrin complexes. Tabariès S, et al., Oncogene. 2011 Mar 17;30(11):1318-28. doi: 10.1038/onc.2010.518. Epub 2010 Nov 15. PMID: 21076473
Claudin-2 promotes colorectal cancer liver metastasis and is a biomarker of the replacement type growth pattern. Tabariès S, et al., Commun Biol. 2021 Jun 2;4(1):657. doi: 10.1038/s42003-021-02189-9. PMID: 34079064
Identification of a Stat3-dependent transcription regulatory network involved in metastatic progression. Ranger JJ, et al., Cancer Res. 2009 Sep 1;69(17):6823-30. doi: 10.1158/0008-5472.CAN-09-1684. Epub 2009 Aug 18. PMID: 19690134
STAT3 Establishes an Immunosuppressive Microenvironment during the Early Stages of Breast Carcinogenesis to Promote Tumor Growth and Metastasis. Jones LM, et al., Cancer Res. 2016 Mar 15;76(6):1416-28. doi: 10.1158/0008-5472.CAN-15-2770. Epub 2015 Dec 30. PMID: 26719528
Les chercheur.es de l'ICG ont mis en place un programme de recherche de renommée mondiale sur les cancers du sein à forte mortalité, y compris les sous-types métastatiques, résistants aux médicaments et rares. Nous sommes des pionniers dans le développement de modèles génétiquement modifiés de sous-types à mauvais pronostic connus sous le nom de cancers du sein HER2-positifs et triple-négatifs (TNBC). Ces modèles ont été utilisés à l'ICG et dans le monde entier pour comprendre comment ces cancers du sein se forment et progressent, conduisant à de nombreuses découvertes importantes et au développement de nouvelles thérapies. Nous avons établi la première biobanque d'échantillons de patientes atteintes du cancer du sein et de données au Québec, désormais partie du Réseau de Recherche en Cancer (RRCancer) soutenu par le FRQS, et un pipeline de recherche en oncologie de précision pour le cancer du sein qui relie le lit du patient et le laboratoire. Cette ressource unique permet de développer des échantillons de patientes en modèles maintenus sous forme de tumeurs vivantes chez les souris (xénogreffes dérivées de patientes) ou cultivées en laboratoire (organoides dérivés de patientes), où nous utilisons une technologie sophistiquée, telle que l'impression 3D de cellules et de composants de la matrice extracellulaire, pour recréer le microenvironnement tumoral. Dans l'ensemble, en combinant notre expertise en modélisation du cancer avec la génomique et les technologies associées, la biologie computationnelle et l'IA, les techniques innovantes de biologie moléculaire et cellulaire, le criblage avancé de médicaments et la génomique fonctionnelle - une approche qui peut inactiver systématiquement chaque gène du génome entier - nous permet de découvrir de nouvelles cibles thérapeutiques pour prévenir la progression et surmonter la résistance dans ces sous-types agressifs de cancer du sein.
Met induces mammary tumors with diverse histologies and is associated with poor outcome and human basal breast cancer. Ponzo MG, Lesurf R, et al. Proc Natl Acad Sci U S A. 2009 Aug 4;106(31):12903-8. doi: 10.1073/pnas.0810402106. Epub 2009 Jul 17. PMID: 19617568
Met synergizes with p53 loss to induce mammary tumors that possess features of claudin-low breast cancer. Knight JF, Lesurf R, et al. Proc Natl Acad Sci U S A. 2013 Apr 2;110(14):E1301-10. doi: 10.1073/pnas.1210353110. Epub 2013 Mar 18. PMID: 23509284
Chemogenomic profiling of breast cancer patient-derived xenografts reveals targetable vulnerabilities for difficult-to-treat tumors. Savage P, et al. Commun Biol. 2020 Jun 16;3(1):310. doi: 10.1038/s42003-020-1042-x. PMID: 32546838
Reduction of Global H3K27me3 Enhances HER2/ErbB2 Targeted Therapy. Hirukawa A, et al. Cell Rep. 2019 Oct 8;29(2):249-257.e8. doi: 10.1016/j.celrep.2019.08.105. PMID: 31597089
Targeting EZH2 reactivates a breast cancer subtype-specific anti-metastatic transcriptional program. Hirukawa A, et al. Nat Commun. 2018 Jun 29;9(1):2547. doi: 10.1038/s41467-018-04864-8. PMID: 29959321
Folliculin impairs breast tumor growth by repressing TFE3-dependent induction of the Warburg effect and angiogenesis. El-Houjeiri L, Biondini M, et al. J Clin Invest. 2021 Nov 15;131(22):e144871. doi: 10.1172/JCI144871. PMID: 34779410
ERRα mediates metabolic adaptations driving lapatinib resistance in breast cancer. Deblois G, et al. Nat Commun. 2016 Jul 12;7:12156. doi: 10.1038/ncomms12156. PMID: 27402251
Le mélanome métastatique est une maladie hautement agressive et difficile à traiter, dont l'incidence augmente malheureusement. La plupart des mélanomes sont causés par des mutations génétiques affectant l'activité d'une voie de signalisation cellulaire spécifique, la voie de signalisation RAS-MAP kinase, qui est un régulateur principal de la croissance, de la division cellulaire et de la survie. Bien que les stratégies de médecine de précision ciblant la voie de signalisation RAS-MAP kinase entraînent des réponses chez de nombreux patients, leur efficacité est inévitablement limitée par la résistance. Les chercheur.es de l'ICG expliquent cette hétérogénéité en menant les études génomiques les plus complètes au monde sur le mélanome métastatique, en utilisant un grand nombre d'échantillons de patients pour cartographier le paysage génomique de cette maladie. À mesure que ces études révèlent de nouveaux sous-types moléculaires et des facteurs génomiques du mélanome, notre recherche fondamentale sur la biologie sous-jacente associe les sous-types moléculaires aux stratégies thérapeutiques ciblées les plus efficaces.
A landscape of driver mutations in melanoma. Hodis E, Watson IR, et al. Cell. 2012 Jul 20;150(2):251-63. doi: 10.1016/j.cell.2012.06.024. PMID: 22817889
Genomic Classification of Cutaneous Melanoma. Cancer Genome Atlas Network. Cell. 2015 Jun 18;161(7):1681-96. doi: 10.1016/j.cell.2015.05.044. PMID: 2609104
The RAC1 P29S hotspot mutation in melanoma confers resistance to pharmacological inhibition of RAF. Watson IR, et al. Cancer Res. 2014 Sep 1;74(17):4845-4852. doi: 10.1158/0008-5472.CAN-14-1232-T. Epub 2014 Jul 23. PMID: 25056119
Dual MAPK Inhibition Is an Effective Therapeutic Strategy for a Subset of Class II BRAF Mutant Melanomas. Dankner M, et al. Clin Cancer Res. 2018 Dec 15;24(24):6483-6494. doi: 10.1158/1078-0432.CCR-17-3384. Epub 2018 Jun 14. PMID: 29903896
Multi-omic analysis reveals significantly mutated genes and DDX3X as a sex-specific tumor suppressor in cutaneous melanoma. Alkallas R, et al. Nat Cancer. 2020 Jun;1(6):635-652. doi: 10.1038/s43018-020-0077-8. Epub 2020 Jun 22.PMID: 35121978
Melanomas with concurrent BRAF non-p.V600 and NF1 loss-of-function mutations are targetable by BRAF/MEK inhibitor combination therapy. Rajkumar S, et al. Cell Rep. 2022 Apr 5;39(1):110634. doi: 10.1016/j.celrep.2022.110634. PMID: 35385748
Le cancer du pancréas est l'un des types de tumeurs les plus agressifs, dépourvu de thérapies efficaces et généralement diagnostiqué à un stade avancé où la chirurgie n'est plus une option curative. La recherche menée à l'ICG, en partenariat avec le Centre universitaire de santé McGill (CUSM) et le Réseau des centres d'oncologie du Marathon de l'espoir de la Fondation Terry Fox, comprend des programmes innovants de génomique, de constitution d'une biobanque et de modélisation à partir de patients. Ces programmes révèlent les facteurs à l'origine de cette maladie mortelle et mettent en lumière les bases génétiques du risque héréditaire du cancer du pancréas. Nos chercheur.es ont mis en place l'Étude québécoise sur le cancer du pancréas (QPCS), une ressource de recherche clinique et translationnelle sur le cancer du pancréas regroupant plus de 1 000 familles ayant des antécédents de cancer du pancréas. Cette étude comprend une banque de connaissances et de spécimens biologiques ainsi qu'une plateforme de modélisation innovante à partir des patients. Grâce à la QPCS et à notre leadership au sein d'initiatives et de consortiums multi-centres canadiens et internationaux à fort impact, notamment le Consortium d'épidémiologie génétique du cancer du pancréas, le Consortium de détection précoce du cancer du pancréas, le Réseau canadien d'oncologie pancréatique (PancOne) et le Profilage amélioré du cancer du pancréas pour des soins individualisés, un programme de recherche translationnelle de l'IRTF, nous favorisons de nouvelles stratégies de médecine de précision pour le cancer du pancréas grâce à la découverte et à la mise en œuvre de biomarqueurs, à des études précliniques de pointe et à des essais cliniques qui font la différence pour les patients.
Oncology clinic-based germline genetic testing for exocrine pancreatic cancer enables timely return of results and unveils low uptake of cascade testing. Wang Y, et al. J Med Genet. 2022 Aug;59(8):793-800. doi: 10.1136/jmedgenet-2021-108054. Epub 2021 Sep 23. PMID: 34556502
A Preclinical Trial and Molecularly Annotated Patient Cohort Identify Predictive Biomarkers in Homologous Recombination-deficient Pancreatic Cancer. Wang Y, et al. Clin Cancer Res. 2020 Oct 15;26(20):5462-5476. doi: 10.1158/1078-0432.CCR-20-1439. Epub 2020 Aug 14
A region-based gene association study combined with a leave-one-out sensitivity analysis identifies SMG1 as a pancreatic cancer susceptibility gene. Wong C, et al. PLoS Genet. 2019 Aug 30;15(8):e1008344. doi: 10.1371/journal.pgen.1008344. eCollection 2019 Aug. PMID: 31469826
Establishing a clinic-based pancreatic cancer and periampullary tumour research registry in Quebec. Smith AL, et al. Curr Oncol. 2015 Apr;22(2):113-21. doi: 10.3747/co.22.2300. PMID: 25908910
Notre capacité à avoir un impact sur la recherche sur les sous-types de cancers rares et à découvrir de nouveaux traitements est illustrée par un programme dynamique sur le carcinome à petites cellules de l'ovaire, type hypercalcémique (SCCOHT), une forme rare de cancer de l'ovaire généralement diagnostiquée chez les femmes de moins de 40 ans, avec une survie à long terme de seulement 30%. En utilisant notre plateforme de modélisation du cancer dérivée des patients, en collaboration avec l'Institut Lady Davis de McGill et des chercheur.es de Grèce, nous avons dérivé un modèle de SCCOHT directement à partir d'un échantillon prélevé chirurgicalement chez une jeune patiente. Appliquant notre expertise de pointe dans la caractérisation fonctionnelle des génomes du cancer, nous avons utilisé ce modèle pour découvrir une cible thérapeutique avec une thérapie ciblée approuvée cliniquement, établissant ainsi une nouvelle stratégie pouvant progresser rapidement vers la clinique. D'autres études ont révélé que d'autres cancers présentant un profil génétique similaire au SCCOHT, notamment certains cancers du poumon, répondaient au même traitement, conduisant à un essai clinique à l'échelle nationale chez les patients atteints de ces cancers.
CDK4/6 inhibitors target SMARCA4-determined cyclin D1 deficiency in hypercalcemic small cell carcinoma of the ovary. Xue Y, et al. Nat Commun. 2019 Feb 4;10(1):558. doi: 10.1038/s41467-018-06958-9. PMID: 30718512
Small-Cell Carcinoma of the Ovary, Hypercalcemic Type-Genetics, New Treatment Targets, and Current Management Guidelines. Tischkowitz M, Huang S, et al. Clin Cancer Res. 2020 Aug 1;26(15):3908-3917. doi: 10.1158/1078-0432.CCR-19-3797. Epub 2020 Mar 10. PMID: 32156746
SMARCA4 loss is synthetic lethal with CDK4/6 inhibition in non-small cell lung cancer. Xue Y, et al. Nat Commun. 2019 Feb 4;10(1):557. doi: 10.1038/s41467-019-08380-1. PMID: 30718506
SMARCA4/2 loss inhibits chemotherapy-induced apoptosis by restricting IP3R3-mediated Ca2+ flux to mitochondria. Xue Y, et al. Nat Commun. 2021 Sep 13;12(1):5404. doi: 10.1038/s41467-021-25260-9. PMID: 34518526